Ion merupakan
atom atau gabungan beberapa atom yang mempunyai muatan listrik positif atau
negatif.
Electron yang
mengelilingi inti atom terus bergerak sambil berputar pada sumbunya. Akan
tetapi, electron dapat meninggalkan atom karena suatu hal, seperti pemanasan,
medan listrik, dan medan magnet. Electron yang keluar dari suatu atom dapat
masuk ke atom lainnya. Akibatnya, atom yang kehilangan electron akan menjadi atom
yang bermuatan listrik positif (ion positif/ kation) karena jumlah proton
menjadi lebih besar daripada jumlah elektronnya, sedangkan atom yang kedatangan
electron menjadi atom bermuatan listrik negative (ion negative/ anoda) karena
jumlah elektronnya melebihi jumlah protonnya.
Peristiwa
terurainya suatu zat menjadi ion-ion disebut ionisasi. Hasil ionisasi disebut ion. Electron yang dapat keluar
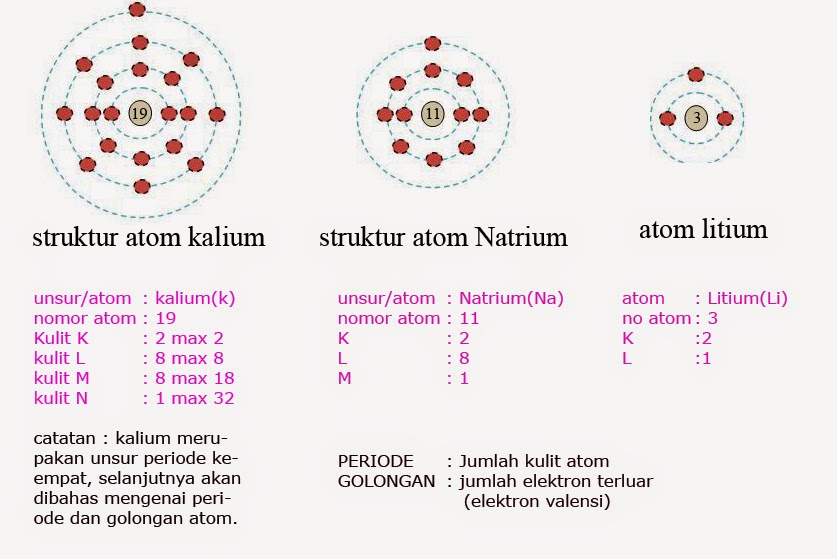
atau masuk ke suatu atom adalah electron yang berada di kulit terluar. Ionisasi
atom hanya terjadi pada atom-atom yang jumlah elektronnya sama dengan 8, 18,
atau 32. Atom-atom yang jumlah elektronnya sama dengan bilangan-bilangan
tersebut sangat sukar terionisasi sehingga disebut unsure gas mulia.
Jumlah electron
yang terlepas atau masuk tergantung pada jumlah electron pada kulit terluar
dengan ketentuan sebagai berikut:
· Jika
jumlah electron terluar kurang dari 4 elektron maka atom ini cenderung
melepaskan electron.
· Jika
jumlah electron terluar antara 4 dan 8 maka atom ini cenderung menerima
electron, jumlah electron yang diterima atau dilepaskan membuat jumlah electron
di kulit itu menjadi 8.
· Jika
jumlah electron pada kulit terluar sama dengan 4 maka atom ini dapat melaepas
atau menerima electron, tergantung dengan unsure apa atom itu berinteraksi.
· Jika
jumlah electron pada kulit terluar sama dengan 8 maka atom itu sangat sukar
melepas maupun menerima electron. Dengan kata lain atom tersebut stabil.
Secara umum, unsure logam lebih
mudah melepaskan elektronnya dibanding unsure nonlogam. Ionisasi juga dapat
terjadi pada zat elektrolit, seperti asam, basa, dan garam. Ada ion yang berupa
partikel atom dan molekul.
Beberapa
contoh kation dan anion dapat kamu lihat pada tabel berikut ini.
Kation
|
Nama
|
Anion
|
Nama
|
Na+
|
Ion
natrium
|
Cl-
|
Ion
klorida
|
Mg2+
|
Ion
magnesium
|
O2-
|
Ion
oksida
|
Al3+
|
Ion
aluminium
|
S2-
|
Ion
sulfide
|
H+
|
Ion
hidrogen
|
I-
|
Ion
iodide
|
K+
|
Ion
kalium
|
CO32-
|
Ion
karbonat
|
Kation
(ion positif) dan anion (ion negatif) dapat bergabung membentuk senyawa ion
yang disebut senyawa ionik. Senyawa ionik dapat menghantarkan listrik. Contoh yang
paling sederhana adalah senyawa natrium klorida atau garam dapur yang terdiri
dari ion Na+ dan ion Cl-. Ion Na+ dan ion Cl-
akan tarik-menarik membentuk suatu senyawa NaCl (garam dapur) karena terdiri
dari dua buah muatan listrik yang berlawanan. Untuk menguraikan senyawa NaCl ini
menjadi unsur-unsur pembentuknya dapat dilakukan dengan cara mengalirkan arus
listrik ke dalam lelehan natrium klorida (NaCl) sehingga NaCl ini akan terurai menjadi
ion Na+ dan ion Cl-.
Berikut adalah video "What are Ions?"
Semoga dapat bermanfaat....

 RSS Feed
RSS Feed Twitter
Twitter


 19.38
19.38
 Unknown
Unknown